研究について
研究紹介 2
当教室では、難治性固形癌である肺癌や膵癌、胃癌などをとりあげ、難治化の要因である転移の分子機構解明とその分子標的治療開発や早期診断法開発に向けたトランスレーショナルリサーチを展開している。
当教室では、難治性固形癌である肺癌や膵癌、胃癌などをとりあげ、難治化の要因である転移の分子機構解明とその分子標的治療開発や早期診断法開発に向けたトランスレーショナルリサーチを展開している。
当教室では、難治性固形癌である肺癌や膵癌、胃癌などをとりあげ、難治化の要因である転移の分子機構解明とその分子標的治療開発や早期診断法開発に向けたトランスレーショナルリサーチを展開している。
肺癌多臓器モデルを用いた転移機構解明と標的分子の探索
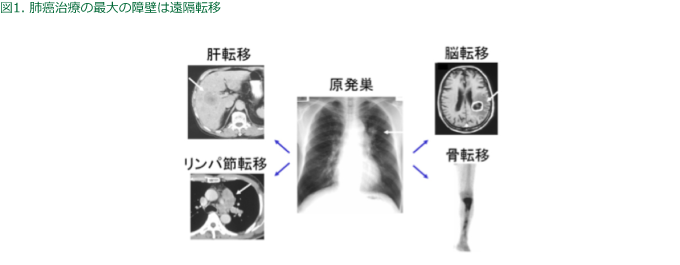
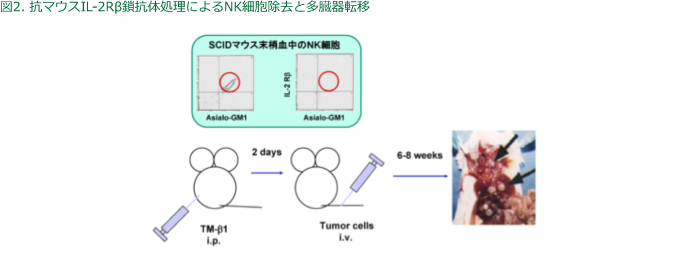
肺癌は多臓器転移を形成することが特徴で、脳、肺、肝、骨、リンパ節などに好発し臓器特異性があることが知られている(図1)。多臓器転移の克服には分子病態解明の基づいた治療標的分子の探索とその制御法の治療効果を検証してゆく必要がある。そのためには臨床を反映し再現性の高い前臨床モデルが必要不可欠である。そこで、ヒト肺癌細胞株をNK細胞除去SCIDマウスに静注することにより肺癌患者の転移様式を反映した多臓器転移モデルを独自に確立した(図2)。さらに、肺癌細胞の増殖・進展に関与する遺伝子発現パターンが臓器間で異なっていることや、宿主側因子としてマクロファージの活性化状態やMMP活性に臓器間較差があり肺癌細胞の転移形成を修飾していることを明らかにし、肺癌をとりまく微小環境の臓器間heterogeneityの存在と転移克服におけるその重要性を示してきた。転移臓器特異的に発現が亢進している遺伝子も同定しており、現在それらの機能解析を進めている。
脳転移の分子機構解明と分子標的治療開発
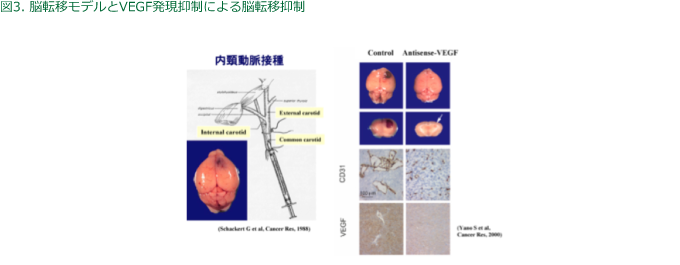
脳転移は肺癌のQOL阻害および予後不良因子であり臨床上特に問題となる。そこで、実体顕微鏡下にマウスの内頸動脈に肺癌細胞を接種し脳転移を形成する再現性の高いモデルを確立した(図3)。さらに、血管新生因子VEGFが腫瘍内の微小血管を拡張させ転移形成を促進する新たな脳転移促進機構が存在することを明らかにしている。現在、血管新生阻害薬の脳転移抑制効果を検討している。
 |
||
骨転移の分子機構解明と分子標的治療開発
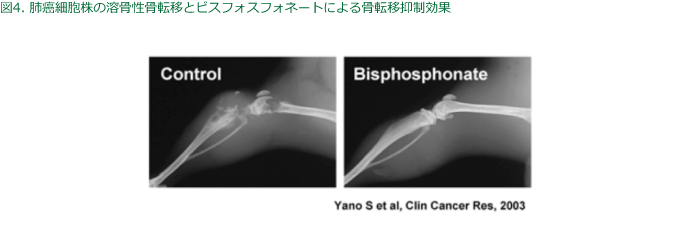
肺癌の骨転移は溶骨性病変を形成することが多いが、約25%の症例においては造骨性病変を形成する。溶骨性骨転移、造骨性骨転移ともに臨床的に患者のQOLを低下させる重要な因子であり、その分子機構の解明と治療法の開発は世界的に注目されている分野である。溶骨性骨転移については、破骨細胞機能を抑制するビスフォスフォネートによる治療が確立されているが、肺癌の造骨性骨転移に対する治療法は無いのが現状である。我々は、肺癌の溶骨性転移モデルおよび造骨性転移モデルをそれぞれ作成し(図4)、分子機構の解明および分子標的治療開発に向けた検討を進めている。
(Yamada T et al, Mol Cancer Ther. 2009)
 |
||























