研究について
がんの転移とは?
癌細胞が発生した場所(原発巣)から移動して、遠隔部位に再び腫瘍を形成することを転移という。早期診断と治療法の進歩により、癌が原発巣に限局するときの治癒率は改善してきているが、遠隔転移が形成された進行例の予後は依然として極めて不良である。したがって、癌を征圧するために転移の制御は必須であり、転移の病態を理解することは重要である。当教室では、我が国の悪性新生物死亡原因の第1位である肺癌を中心とした固形癌の転移の分子機構の理解に基づいた分子標的治療の開発を目的に研究を展開している。
I. 転移研究の歴史
転移という言葉は、1829年にフランスのRecamierが最初に使ったとされるが、1973年にFidlerらが低転移性のマウス黒色腫B16細胞から高転移性細胞の選択に成功し、それを用いた転移実験モデルを確立したことにより転移研究の基礎が築かれた。また、1986年にはLiottaにより浸潤が癌細胞と基底膜の接着、基底膜成分の分解、癌細胞の運動の3段階によって遂行されるという「Three Step Theory」が提唱された。このような癌転移の概念および実験系の確立が起爆剤となり、転移メカニズムを細胞および分子レベルで解明する研究が急速に展開されるようになった。その結果、1)癌細胞は生物学的に不均一(heterogenous)であること、2) 癌細胞は絶えざる遺伝子変異の結果転移に好都合な細胞形質を獲得し、ごく少数の転移能を有した癌細胞が転移の過程で選択され増えていくこと、3)転移の全ての過程が正常細胞と癌細胞の複雑な相互反応の上に成り立っており、接着分子、蛋白分解酵素、増殖因子、血管新生因子、ケモカインなど多くの分子が関与していることなどが明らかになってきた。また、癌の転移は決してランダムに偶然おこるわけではなく、下記に示す転移の過程を連続して全てクリアした癌細胞のみ(数百万個に1個程度と推測されている)が形成することができるため、Fidlerは転移した癌細胞はオリンピックの10種競技のチャンピオンに例えている。
II. 転移のメカニズム
転移には血行性転移、リンパ行性転移、管腔性転移(たとえば細気管支肺胞上皮癌の経気管支転移)などがあるが、そのメカニズムは基本的には似通っているため、血行性転移を例にとり概説する。血行性転移は、癌細胞の1)原発巣での増殖、2)原発巣からの癌細胞の離脱と脈管(血管やリンパ管)への浸潤、3)脈管内での移動、4)転移臓器の血管内皮への接着、5)転移臓器への浸潤、6)転移臓器内での増殖などの過程から構成されており(図6)、すべての過程が連続的に起こった結果生じる。また、全ての過程において癌細胞は免疫排除機構から逃れて生存する必要がある。
 |
||
1. 原発巣での増殖
「増殖なくして転移なし」といわれるように、転移を形成するためにはまず癌細胞が原発巣で増殖する必要がある。原発巣での増殖には様々な増殖因子とその受容体がオートクラインまたはパラクライン的に関与していると考えられる。代表的な因子としてEGF(epidermal growth factor)受容体がある。EGF受容体は多くの固形癌に過剰発現されており、リガンド(TGF-a:transforming growth factor-aとEGFなど)が細胞外ドメインに結合すると、細胞内ドメインのチロシンキナーゼがリン酸化され細胞内シグナル伝達の結果DNA合成が刺激され、癌細胞の増殖を促進する。さらに、癌が1-2mm以上の大きさに増大するためには酸素や栄養を運ぶ血管の新生が必須であるが、血管新生も種々の血管新生促進因子と抑制因子により制御されている。血管新生については他稿で詳述されているので参照されたい。
2. 原発巣からの癌細胞の離脱と脈管への浸潤
増殖した癌細胞は次に原発巣から離脱する必要がある。これに関与する重要な分子としてE-カドヘリンが知られている。E-カドヘリンは細胞膜貫通蛋白であるが、細胞内裏打ち蛋白であるカテニンを介して細胞骨格に結合している。細胞外ドメインの先端で隣接する細胞のカドヘリンと結合することで細胞接着が生じる。すなわちE-カドヘリンは接着剤としての機能を果たしていて、その機能が失われると細胞同士の結合能力が失われる。高浸潤性の癌ではE-カドヘリンが低下し、原発巣から癌細胞が離脱しやすいと考えられている。
癌細胞が原発巣から離脱してもその周辺には細胞外マトリックス(ECM:extracellular matrix)が存在し、細胞の移動を妨げている。ECMは上皮下の間質結合組織とその境界面に膜状に存在する基底膜からなる。ECMは、各種コラーゲン、フィブロネクチン、ラミニンなどの糖蛋白質、プロテオグリカンなどを含んでいるが、主に基底膜はIV型コラーゲンで、間質はI型コラーゲンで構成されている。癌細胞は自身または間質細胞が産生する各種プロテアーゼやグリコシダーゼを利用してECMを分解し、生じた隙間を移動する。さらにECMへの接着、分解、移動を繰り返すことにより組織浸潤が達成される。これはECMとの接着にはインテグリンを中心とする接着分子が、ECMの分解には各種のプロテアーゼ(メタロプロテアーゼ、セリンプロテアーゼ、システインプロテアーゼ、アスパラギン酸プロテアーゼ)が関与しているが、その中でもメタロプロテアーゼ(MMP)が中心的役割を演じている。
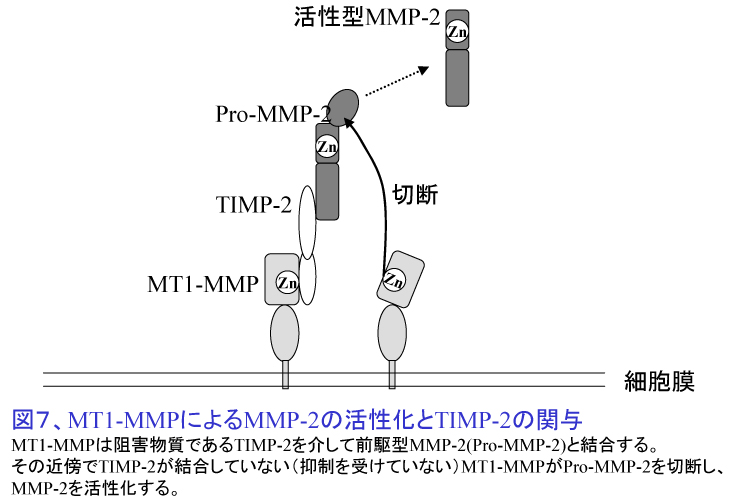
MMPは金属イオン要求性蛋白分解酵素で、25種類以上が同定されている。MMP存在様式の違いから分泌型と細胞膜型とに分類される。分泌型MMPはほとんどが細胞外に非活性型として分泌され、間質あるいは細胞表面プラスミンやトロンビンなどにより活性化され酵素作用を発揮する。よって、産生細胞から離れた広範囲のECMの分解が可能と考えられる。一方、膜型MMPは産生細胞の細胞膜表面に局在し、その近傍の基質を限定的に分解する。MMPの活性は、その発現量、活性化機構、あるいは生体におけるMMP抑制因子TIMP1-4との分子バランスなどによって厳密に制御されている。たとえば、膜型MMPのプロトタイプであるMT1-MMPは、代表的分泌型MMPであるMMP-2とTIMP-2をアダプターとして間接的に結合し、MMP-2を活性化する(図7)。これらの分子は癌細胞よりもむしろ線維芽細胞などの間質細胞が高発現し、癌の浸潤を促進していると考えられている。
 |
||
3. 脈管内での移動
血管内に侵入した癌細胞は、血流の機械的ストレスやナチュラルキラー(NK)細胞を中心とした免疫系の攻撃により大部分が短時間で死滅すると考えられている。したがって、短時間に血管外に脱出あるいは少なくとも血管内皮細胞に接着した癌細胞のみが生存し転移することができる。また、高転移性細胞は癌細胞同士あるいは血小板とともに集塊を形成し生存に有利な環境を形成することがある。
4. 転移臓器の血管内皮への接着
集塊を形成した癌細胞が毛細血管に塞栓を形成する場合と、癌細胞と血管内皮細胞が特異的結合により接着する場合がある。後者の場合、複数の糖鎖や接着分子が利用され巧妙に接着が制御されており、使用される糖鎖や接着分子の種類により転移の臓器特異性の一部が規定されていると考えられる。その齬痰ニしては、まず癌細胞表面のシアリルLexやシアリルLea抗原などの糖鎖と、その受容体である血管内皮細胞上のセレクチン(E-セレクチン、P-セレクチン)との弱い接着が誘導され、それに続いて癌細胞が発現するLFA-1やVLA-4などのインテグリン分子が血管内皮細胞のICAM-1やVCAM-1などの接着分子とより強固な結合をする機構がある。また、癌種によってはCD44やCXCR4などのケモカインレセプターが血管内皮細胞への接着に重要な役割を果たしている。
5. 脈管外への脱出
癌細胞は血管内皮細胞同士の接着に割り込み、その下層構造である基底膜にインテグリンなどを介して接着し、基底膜成分のIV型コラーゲンやラミニンを分解し、移動する。その際、細胞とECMの接着部位には接着斑(focal adhesion)と呼ばれる構造が形成され細胞内の細胞骨格蛋白がインテグリンを介してECMと連結する。この接着斑において方向性のある接着・脱接着が繰り返され、一定方向に細胞が運動していくと考えられている。
6. 転移巣での増殖
原発巣での増殖同様、種々の増殖因子や増殖因子受容体、血管新生因子が関与するが、臓器特異的に産生される因子により臓器特異性が規定されうる。たとえば、IGF-1 (insulin-like growth factor-I)は多くの臓器で発現されているが肝で最も高発現している。IGF-1は細胞周期を促進するため、IGF-1受容体を発現した癌細胞の肝での増殖を特異的に促進する可能性がある。同様に、肝ではEGFRのリガンドであるTGF-aの発現が高く、EGFRを発現した癌細胞の増殖を促進していると考えられる。
腫瘍が原発臓器にとどまっていれば外科的切除で治癒が期待できることや脈管への浸潤から転移臓器の血管内皮への接着の過程は数時間から数日の間に完成されると考えられていることから、転移臓器における腫瘍増大を阻止する治療法をいかに開発するが転移治療の鍵になると思われる。
III. 転移研究のトピックス
1. 癌細胞の運動能獲得
元来正常細胞は位置移動しないが、癌細胞は悪性度が高まるにつれ上皮様(epithelial)の状態から線維芽細胞様の間葉(mesenchymal)の状態(上皮−間葉移行:epithelial-mesenchymal transition:EMT)へ、さらには間葉(mesenchymal)の状態からアメーバー様(amoeboid)への状態(間葉−アメーバー様移行:mesenchymal-amoeboid transition; MAT)へ形態を変化させることにより浸潤運動能を獲得することが明らかになってきた(図8)。EMTはE-カドヘリン-b カテニン系の機能喪失により、集団を形成している癌細胞が単細胞で遊走することを可能にしている。MATは、プロテアーゼ阻害薬存在下でECM分解ができない状態において、癌細胞がアメーバー様に変化することでプロテアーゼ非依存的に運動することを可能にしている。EMTやMATは、癌細胞が進展してゆくために行う一種の適応と考えられ、現在その分子機構を明らかにする研究が盛んに行われている。
 |
||
2. 転移の臓器特異性
癌種によって特徴的な転移臓器のパターンを示すことは臨床上よく経験するところであり転移の臓器特異性(organ tropism)と呼ばれている。転移の臓器特異性は、癌細胞を運ぶ血行動態と、癌細胞がある臓器で選択的に増殖しうる特性という2つの要素が関係している。臨床的には両方の要素が部分的に関与しあっている場合が多いと考えられ、相矛盾するものではない。前者は1928年にEwingより提唱された「転移の臓器特異性は血流の方向のみにより規定される」という考え方でanatomical-mechanical theoryとよばれている。消化器癌の肝転移はこの説がよく適合すると考えられる。後者は、1889年にPagetにより提唱されseed and soil theoryとよばれている。植物の種はいろいろな場所に植えられることができるが、それに適した土壌でのみ発育、成長することが可能であることから、癌細胞を種(seed)に、転移臓器を土壌(soil)になぞらえて、「癌の転移の成立は癌細胞の増殖に適した微小環境を有する臓器にのみ可能である」という考えである。近年、その分子機構が徐々に明らかになってきた。
1)ケモカインと臓器特異性
ケモカインは細胞に対して走化性(chemotaxis)を引き起こし、細胞間の相互反応を媒介するサイトカインで炎症反応を媒介する中心的因子である。ケモカインにはよく保存された4つのシステイン残基が存在し、N末端側に存在する2つのシステイン残基の間に存在するアミノ酸残基数により、CXC, CC, C, CX3Cケモカインの4つのサブファミリーに分類され、45種類以上が同定されている。ケモカイン受容体も20種類以上同定されている。
最近、(1)CXCR4を発現する癌細胞が、そのリガンドであるCXCL12を高発現するリンパ節、骨髄、肺に選択的に転移すること、(2)CCR7を発現する癌細胞が、そのリガンドであるCCL19, CCL21を高発現するリンパ節に転移すること、(3)癌間質中の線維芽細胞がCXCL12を産生して血管内皮細胞前駆細胞を癌組織中に呼び込むとともに、癌に対する増殖因子として働くことにより腫瘍進展に関与することが報告されたことにより、ケモカインやその受容体が転移の臓器特異性規定因子として注目され、それらの阻害薬による転移抑制効果が期待されている。
2) 網羅的遺伝子解析による転移関連因子の探索
DNAマイクロアレイによる網羅的遺伝子解析やプロテオミクスによる網羅的蛋白解析が可能となり、2002年頃より癌の遠隔転移・再発に関係する遺伝子発現パターンが同























